pH-Wert
Für den interessierten Leser hier die Bedeutung der Abkürzung und Definition des Begriffes pH-Wert. pH bedeutet pondus Hydrogenii und definiert den „negativen dekadischen Logarythmus der Wasserstoffionen-Konzentration“. Der pH-Wert ist eine dimensionslose Zahl.
Wie schon in der Rubrik Salze, Mineralstoffe, etc. ausgeführt unterliegen Säuren und Laugen in wässriger Lösung der Dissoziation. Säuren sind durch das H+-Ion, auch Proton genannt charakterisiert, wogegen Laugen oder Basen sich durch das OH–Ion, auch Hydroxidion genannt, auszeichnen. Vereinfacht kann gesagt werden, dass der pH-Wert das Verhältnis von Säuren und Laugen wiederspiegelt. Sind gleiche Ladungsmengen Protonen und Hydroxidionen vorhanden so beträgt der pH-Wert 7, überwiegen die Protonen wird die Lösung als sauer bezeichnet, überwiegen aber die Hydroxidionen wird die Lösung als basisch oder auch alkalisch bezeichnet.
Wie Abb. 4 zeigt reicht die pH-Skala von pH 0, stark sauer, bis pH 14, stark alkalisch, wobei der Neutralpunkt bei pH 7 liegt,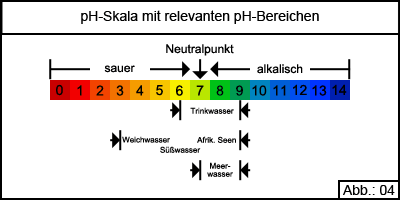 die Lösung also weder sauer noch alkalisch reagiert. Geht man davon aus, dass auch Wasser der Dissoziation unterliegt und in ein Proton und ein Hydroxidion aufgespalten wird, ergibt sich hieraus, dass Wasser einen pH-Wert von 7 haben sollte. Dies trifft aber nur auf reines, destilliertes Wasser unter Luftabschluss zu! Sobald Wasser der Luft ausgesetzt wird, nimmt dieses Kohlendioxid (CO2) aus der Luft auf und reagiert zum Teil nach folgender Gleichung zu Kohlensäure (H2CO3). CO2 + H2O <==> H2CO3. Durch diesen Vorgang nimmt das Wasser einen leicht sauren Charakter an und zeigt einen pH-Wert von ca. 5,3. Wie sich aus der Definition des pH-Wertes ergibt, verläuft die pH-Skala logarhitmisch.
die Lösung also weder sauer noch alkalisch reagiert. Geht man davon aus, dass auch Wasser der Dissoziation unterliegt und in ein Proton und ein Hydroxidion aufgespalten wird, ergibt sich hieraus, dass Wasser einen pH-Wert von 7 haben sollte. Dies trifft aber nur auf reines, destilliertes Wasser unter Luftabschluss zu! Sobald Wasser der Luft ausgesetzt wird, nimmt dieses Kohlendioxid (CO2) aus der Luft auf und reagiert zum Teil nach folgender Gleichung zu Kohlensäure (H2CO3). CO2 + H2O <==> H2CO3. Durch diesen Vorgang nimmt das Wasser einen leicht sauren Charakter an und zeigt einen pH-Wert von ca. 5,3. Wie sich aus der Definition des pH-Wertes ergibt, verläuft die pH-Skala logarhitmisch.
Werden z. B. 400mg Stoff XYZ benötigt, um den pH-Wert von pH 7 auf pH 6 zu senken, so werden die zehnfache Menge, also 4000mg XYZ benötigt, um eine Senkung von pH 7 auf pH 5 zu bewirken. Hieraus ergibt sich, dass Änderungen des pH-Wertes und sei es auch „nur“ um eine pH-Stufe, erheblichen Einfluss auf die Wasserbeschaffenheit und somit auf das Wohlbefinden der Fische haben können. Im Bereich der Aquaristik und der damit verbundenen Wasserchemie kann verallgemeinert gesagt werden, dass der pH-Wert größtenteils durch das im Wasser gelöste CO2, also die Kohlensäure und durch gelöste Salze bestimmt wird. Der pH-Wert ist eine Summengröße und gibt keinerlei Auskunft darüber, durch welche Stoffe dieser gebildet wird. Daraus ergibt sich aber auch, dass es für die Belange der Aquaristik wichtig ist, durch welche Stoffe ein bestimmter pH-Wert erreicht wird. Einen pH-Wert von 6,1 kann durch Zugabe von Essigsäure zu destilliertem Wasser erreicht werden, wobei kein Fisch in diesem Wasser existieren könnte. Der gleichen pH-Wert kann aber auch durch das Auflösen einer Salzmischung in destilliertem Wasser erreicht werden, wodurch ein Wasser entstehen kann, das für Aquarienfische optimal geeignet ist. In der Aquaristik hat der pH-Wert nicht die zentraler Bedeutung die ihm immer zugeschrieben wird und muss immer im Zusammenhang mit der Karbonathärte und dem im Wasser gelösten CO2 gesehen werden (Siehe hierzu auch Wasserhärte und Puffersystem).
Weiterhin kann der pH-Wert auch dafür verantwortlich sein, ob ein bestimmter Stoff in einer harmlosen, oder für Fische sehr giftigen Form vorliegt. So fallen beim sogenannten Stickstoffabbau im Aquarium Ammoniumionen NH4+ als Zwischenprodukt an. Diese reagieren, abhängig vom pH-Wert, nach folgender Gleichung: NH4+ + OH- <==> NH3 + H2O. Ab einem pH-Wert von ca. 7,5 wandelt sich das relativ ungiftige Ammonium in hochgiftigen Ammoniak um, wobei ab einem pH-Wert von ca. 9,5 das Ammonium nahezu vollständig in Ammoniak umgewandelt ist. Wie der Doppelpfeil (<==>) ausdrückt, ist dieser Vorgang reversiebel, also umkehrbar, und kann somit leicht durch entsprechende Anpassung des pH-Wertes, auf der Seite des ungiftigen Ammoniums gehalten werden.
Abschließend kann zu Bedeutung des pH-Wertes in der Wasserchemie gesagt werden, dass diesem zwar eine gewisse Aufmerksamkeit geschuldet werden sollte, dieser aber auch immer im Zusammenhang mit anderen wichtigen Komponenten, wie z. B. Wasserhärte und CO2-Gehalt gesehen werden muss.
